El proceso de registro y certificación para exportar dispositivos médicos a Corea del Sur.
en aduanas y problemas de cumplimiento.
eficiente y seguridad en pagos.
Corea del SurEl proceso de acceso al mercado es relativamente complejo e implica varios pasos y la participación de múltiples departamentos.En este artículo se presentará brevemente el proceso de certificación y registro necesario para exportar dispositivos médicos a Corea del Sur.
autoridad competente
La Administración de Alimentos y Medicamentos de Corea (MFDS) es la autoridad competente en Corea para los dispositivos médicos,responsable de los alimentos,medicamentos,dispositivos médicos yla seguridad,el desarrollo de las industrias alimentaria y farmacéutica,así como la promoción de la salud pública.
Clasificación de dispositivos médicos
Corea clasifica los dispositivos médicos en cuatro categorías: I,II,III y IV,un sistema muy similar al utilizado por la Unión Europea.Cada categoría tiene su propia vía de acceso al mercado y,según la clasificación de riesgo del dispositivo,los procedimientos y tiempos de aprobación también varían.
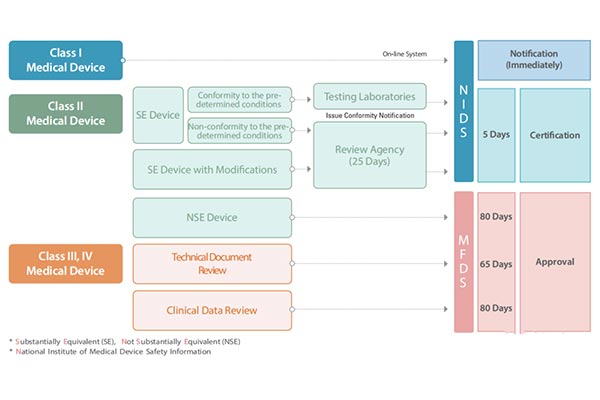
Pruebas del producto y ensayos clínicos
Las muestras de productos que requieren registro pueden enviarse directamente al laboratorio en Corea para su prueba o evaluarse en un laboratorio nacional que cuente con la acreditación correspondiente en Corea,presentando un informe de prueba que acredite su conformidad.La MFDS ha designado una serie de laboratorios de ensayo y hospitales específicos para la realización de ensayos clínicos.
Evaluación del sistema
Los fabricantes de dispositivos médicos de clase II,III y IV que exporten a Corea deben cumplir con los requisitos de KGMP (Korean Good Manufacturing Practice),los cuales son similares a los de la ISO 13485.El certificado KGMP se otorga al importador y no al fabricante,y se renueva cada 3 a?os.
Sitio web de solicitud de certificados de cosméticos de Corea:
Proceso de registro de dispositivos médicos en Corea
Los dispositivos médicos importados de Corea se dividen en los siguientes pasos: selección del titular coreano,registro del producto,preparación de la documentación,pruebas del producto,ensayos clínicos,certificado de registro del producto,preparación de la documentación KGMP y acceso hospitalario.
Lanzamiento del producto y supervisión posterior a su comercialización
Después de que se emiten el Certificado de Registro del Producto y el Certificado KGMP,para los dispositivos médicos que no sean de uso doméstico también es necesario completar el proceso de admisión hospitalaria,ingresar al sistema de seguro médico del hospital y obtener el número de seguro médico hospitalario.A partir de entonces,el producto puede comercializarse oficialmente en el mercado coreano.Una vez que el producto esté en el mercado,la MFDS tiene la autoridad para dar seguimiento a algunos dispositivos médicos de alto riesgo designados.Los productos que presenten reacciones adversas en el mercado coreano deben ser retirados oportunamente.
Por último,los requisitos para que un producto extranjero ingrese al mercado coreano son: se debe preparar una documentación técnica muy detallada y la información necesaria para solicitar el KGMP de Corea; el sistema de la empresa debe cumplir con los requisitos de la ISO 13485; y el producto debe cumplir con los estándares correspondientes.Lo anterior corresponde al sistema de acceso para dispositivos médicos en Corea,esperando que sea de utilidad para los dispositivos médicosEs útil para las empresas.
?Te ha sido útil? ?Danós un "me gusta"!
Consulte a nuestros asesores para auditoría, cotización y despacho aduanero integral.

Comentarios recientes (0) 0
Deja un comentario